مرکز جامع دامپزشکی ایران
iranvetmed.irمرکز جامع دامپزشکی ایران
iranvetmed.irتولد دو خوک با استفاده از مهندسی ژنتیک سلول میمون؛ کایمراها آینده پیوند اعضا در انسانی
برای اولین بار در جهان، در چین و بعد از ایجاد تغییرات ژنتیکی در سلول های بنیادین سینومولگوس میمون در طبیعت، دو خوک بدنیا آمدند. کایمراهای میمون-خوک بدنیا آمده که حیوانات جدیدی با سلول هایی از دو حیوان مختلف هستند- تنها یک هفته زنده ماندند.

کایمرا به موجودی اطلاق می شود که ترکیبی از دو یا چند جانور متفاوت باشد. تانگ های، یکی از محققان چینی این پروژه که در آزمایشگاه کلیدی دولتی سلول های بنیادین و زیست شناسی زایشی در پکن کار می کند در این باره چنین گفته است: «این اولین گزارش از کایمراها خوک-میمون است که با طی دوره بارداری کامل به دنیا می آیند».
برای اولین بار در جهان، در چین و بعد از ایجاد تغییرات ژنتیکی در سلول های بنیادین سینومولگوس میمون در طبیعت، دو خوک بدنیا آمدند.
اوایل سال جاری، محققان ژاپنی موفق به رشد پانکراس انسان در یک موش شدند که گامی بزرگ در زمینه مطالعه کایمراها یا ارگانیسم هایی که سلول های از دستکم دو گونه زیستی متفاوت داشته باشند به شمار می آمد. این هیبریدهای ژنتیکی مورد آزمایش و بررسی قرار می گیرند زیرا هدف نهایی رشد تمامی ارگان های بدن در درون بدن دیگر حیوانات است تا بعدها بتوان این اندام ها را به بدن انسان پیوند زد و بدین ترتیب مشکل پیوند اعضا در انسان به طور کامل رفع شود. در مورد کایمراهای میمون-خوک، محققان تغییراتی ژنتیکی را در سلول های میمون در مرحله بارورسازی آزمایشگاهی اعمال کردند و در ادامه موفق به ساخت پروتئینی به نام GFP شدند.
برای اولین بار در جهان، در چین و بعد از ایجاد تغییرات ژنتیکی در سلول های بنیادین سینومولگوس میمون در طبیعت، دو خوک بدنیا آمدند.
این پروتئین دارای نور فلوئورسنت شده و به محققان اجازه می داد که سلول های میمون و دیگر سلول های منشعب شده از آن را ردیابی کنند. در ادامه تیم تحقیقاتی موفق شد که سلول های بنیادین جنینی را جداسازی کرده که بعدها در جنین خوک هایی که تنها ۵ روز از باروری آن ها می گذشت تزریق شدند. در مجموع، ۴٫۰۰۰ از این جنین ها در رحم خوک های ماده کاشت شد. در نهایت ۱۰ نوزاد خوک متولد شده که تنها دو نمونه کایمرا بوده و دارای سلول های میمون بودند. در این کایمراها، بافت های قلب، کبد، ریه و طحال دارای مقادیری از سلول های میمون بودند اگر چه این درصد بسیار کم بوده و در حدود یک در هزار و یک در ده هزار برآورد شد.
برای اولین بار در جهان، در چین و بعد از ایجاد تغییرات ژنتیکی در سلول های بنیادین سینومولگوس میمون در طبیعت، دو خوک بدنیا آمدند.
تنها بعد از یک هفته، تمامی بچه خوک ها مردند، اعم از کایمرا و غیرکایمرا. محققان گفتند که در حال حاضر اطلاعات دقیقی از علت مرگ این بچه خوک ها ندارند اما احتمال می دهند این موضوع در اثر عوارض فرآیند بارورسازی در آزمایشگاه و نه ماهیت کایمرایی بودن آن ها بوده باشد. این مشکل بدان دلیل رخ می دهد که بارروری آزمایشگاهی در خوک ها به خوبی و موفقیت این رویکرد در مورد انسان ها و دیگر حیوانات نیست. به گفته های، این تیم تحقیقاتی در ادامه قصد دارد حیوانات سالمی را با سهم بیشتری از سلول های میمون تولید کند. اگر این تحقیق با موفقیت همراه شود، آن ها سعی خواهند کرد خوک هایی تولید کنند که با یک ارگان کامل ساخته شده از سلول های یک نخستی (مانند میمون) بدنیا آمده باشد. البته صحبت در این مورد آسان تر از انجام و موفقیت آن است.
برای اولین بار در جهان، در چین و بعد از ایجاد تغییرات ژنتیکی در سلول های بنیادین سینومولگوس میمون در طبیعت، دو خوک بدنیا آمدند.
در سال ۲۰۱۷، یک تیم تحقیقاتی دیگر در کالیفرنیا با موفقیت یک کایمرای خوک-انسان تولید کرد اما تعداد سلول های انسان در کایمرای نهایی تنها ۱ در ۱۰۰٫۰۰۰ سلول بود. و به دلایل اخلاقی، جنین ها تنها برای یک ماه رشد داده شند زیرا نگرانی هایی در این مورد وجود داشت مبنی بر اینکه ممکن بود مغز نوزاد خوک نهایی نیمه انسانی باشد. همچنین منتقدانی نسبت به این رویکرد نیز وجود دارند. پل نوپفلر، یک زیست شناس سلول های بنیادین در دانشگاه کالیفرنیا، بر این باور است که رشد ارگان های انسانی مناسب پیوند در بدن کایمراهای انسانی-حیوانی غیرممکن است. وی در این باره چنین می گوید: «با توجه به کارآمدی بسیار پایین کایمرایی و مرگ تمامی این حیوانات، من حقیقتاً این موضوع را بسیار ناامید کننده می بینم».
از نظر شما آیا خلق کایمراها و رشد اندام های انسانی در بدن حیوانات اخلاقی است و می تواند عواقب ناخوشایندی در پی داشته باشد یا خیر. نظرات خود در این مورد را با ما و دیگر مخاطبان روزیاتو در میان بگذارید.
ماهی قرمز چگونه با محیط آکواریوم کنار میآید؟
مجله ایلیاد/ برای بیشتر موجودات زنده، به ویژه آنهایی که تنفس متفاوتی دارند، زندگی بدون منبع اکسیژن خوب، چندان جالب نیست. ماهی قرمز، استثنای عجیب و غریبی است. ماهیهای گونهیCarassius در زمانهای نامطلوبی که محیط اطراف دچار کمبود اکسیژن میشود، روشی شسته و رفته دارند که منجر به بقای آنها میشود؛ آنها الکل درست میکنند. اکنون میدانیم چگونه این کار را انجام میدهند.

در کتاب زیست شناسی ۱۰۱ یاد میگیریم که اکسیژن با «گلوکز کربوهیدرات» ترکیب میشود تا «دیاکسیدکربن» و آب تولید کند و برای ما انرژی فراهم کند. آب نسبتأ سودمند است، درحالیکه دیاکسیدکربن محصولی فرعی است، در محیطزیست رها میکنیم. گاهی اوقات، بافتهای ما از منبع اکسیژن محلیشان خالی میشوند، مثل زمانی که سخت ورزش میکنیم یا زمانیکه محیطزیست موقتأ دچار کمبود اکسیژن میشود.
برای غلبه بر این کمبود، بیشتر حیوانات مثل ما مسیرهای آنزیمی دارند که میتوانند کمی انرژی از گلوکز بدون اکسیژن بهدست آورند. متأسفانه، این کار ما را با مادهای تند و زننده بهنام «لاکتیک اسید» تنها میگذارد. لاکتیک اسید، در نهایت در کبد به گلوکز تبدیل میشود، اما این فرآیند نیز به اکسیژن نیاز دارد. به عبارت دیگر، این فقط یک راه حل کوتاه مدت است. اگر لاکتیک اسید همچنین ایجاد شود، باعث «اسیدوز لاکتیک» میشود؛ وضعیتی که pH بافتها را پایین میآورد و همهی مشکل را ایجاد میکند.
ماهی قرمز، نباید نگران این قضیه باشد. بهمدت چندین دهه، مشخص شده که این حیوان خانگیِ چندین ساله استعداد دارد لاکتیک اسید را به مولکولی کمخطرتر، یعنی الکل تبدیل کند. برخلاف لاکتیک اسید، اتانول به آسانی به آب تبدیل میشود، از میان آبشش ماهی عبور میکند.
هیچ مهرهدار دیگری این توانایی را ندارد و در نتیجه دانشمندان در دانشگاههای اوسلو و لیورپول تصمیم گرفتند اسرار ماهی کپور را کشف کنند. قضیه به ۸ میلیون سال پیش بر میگردد؛ زمانی که اجداد ماهی قرمز و کپور نسخههایی از ژنهای مسئول مجموعهای چند آنزیمی «دهیدروژناز پیرووات» را ایجاد کردند.
ژنهای اصلی، وظیفهی اصلیشان برای تهیهی مشتقی از گلوکز بهنام پیرووات را حفظ کردند تا وارد چرخهی متابولیکی شوند که انرژیزا است. در عین حال، نسخههای این ژنها در طول زمان به آسانی تغییر کردند و تکامل پیدا کردند تا آنزیمی شبیه به آنزیم موجود در مخمر آبجو بسازند که «اسید پریکوئیک» را به «استالدئید» یا اتانال تبدیل کند و سپس به اتانول تبدیل شود. این ماهی نیز همانند مهرهداران دیگر معمولأ از همین مسیر استفاده میکند و اکسیژن را از طریق آبششهایش جذب میکند تا در تنفس هوازی استفاده کند.
وقتی اکسیژن کم باشد، این مسیر تغییر میکند تا اتانول تولید کند. اکسیژن کافی نیست، اما ماهی کپور میتواند بهمدت چندین ماه در اعماق باقی بماند تا وضعیت بهتر شود. محقق ارشد، «کاترین الیزابت فاگرنس» از دانشگاه اوسلو گفت: «این تحقیق بر نقض تکثیر کل ژنوم در تکامل نوآوری بیولوژیکی و سازگاری گونهها با محیطهای غیرقابل سکونت تأکید دارد.»
ماهی قرمز، در خانهی شما به نظر به دور قلعهای شنی درون آکواریوم میچرخد، اما اجداد وحشیاش باید با دورههای زمستان طولانی در آبهای تقریبأ یخزده کنار میآمدند. محقق «مایکل برنبریک»، فیزیولوژیست تکاملی در دانشگاه لیورپول، گفت: «در آبهایی با اکسیژن آزاد در استخرهایی پوشیده از یخ که به مدت چندین ماه در زیستگاههای شمال اروپا طول میکشید، غلظت الکل در خون ماهیهای کپور میتواند به بیش از ۵۰ میلیگرم در ۱۰۰ میلیلیتر برسد که این مقدار بالای محدودهی شیرجه در آب آشامیدنی در این کشورها است.»
وی افزود: «هرچند این وضعیت هنوز خیلی بهتر از مواجهه با لاکتیک اسید است که محصول نهایی متابولیکی مهرهداران دیگر از جمله انسانها در زمان از دست دادن اکسیژن است. همچنین میتواند توضیح دهد که چرا ماهی قرمز در مخازن آب سرد و کم اکسیژن در اکواریومها میتواند، دوام بیاورد. آنها به حدی الکل مصرف میکنند که چیزی متوجه نمیشوند! جدا از درک تغییر بیولوژیکی ناگهانی خارقالعادهی این ماهیها، تحقیقات نوعی تغییرِ تکاملی در عملکرد یک صفت را از طریق تکثیر نشان میدهد.»
معمولأ عملیات مهمی مثل تنفس نمیتوانند وظایف خود را تغییر دهند. در این صورت، داشتن نسخهای واقعأ مفید است.
این باکتری کُشنده ، به آنتی بیوتیک مقاوم است
ایسنا/ متخصصان استرالیایی به تازگی موفق به کشف نوعی از سویه مقاوم به آنتیبیوتیکِ باکتری "شیگلا" شدهاند که عامل بروز نوعی عفونت باکتریایی است و از طریق مدفوع پخش میشود و هر ساله نیز جان بیش از نیم میلیون نفر را در جهان میگیرد.
در مطالعهای که اوایل ماه جاری میلادی توسط متخصصان علوم پزشکی دانشگاه ملبورن منتشر شد، ۱۸۴ نمونه از باکتریهای جداگانه مقاوم در برابر داروها در ۱۲ بیمار زن و ۱۷۲ بیمار مرد در ایالت ویکتوریای استرالیا شناسایی شدند.
به گفته متخصصان، گونه باکتری شیگلا که آنها شناسایی کردهاند، در برابر آنتیبیوتیکهای خوراکی کاملاً مقاوم بوده و در عوض باید با آنتیبیوتیکهای داخل وریدی که در بیمارستانها عرضه میشود، درمان شود.
کشف سویهای از باکتریهای شیگلا که با دارو درمان نشده و نیاز به بستری شدن دارد، منجر به نگرانی بسیاری از متخصصان شده است. این در حالی است که متخصصان باید درمان آنتیبیوتیکی را برای افرادی حفظ کنند که در شرایط اولویت قرار دارند، برای مثال افرادی که سیستم ایمنیشان سرکوب شده یا افرادی که دارای بیماریهای شدید هستند.
متخصصان توصیه میکنند که نمونههایی از مدفوع پس از تشخیص شیگلوز برای کشت و آزمایش حساسیت به آنتیبیوتیکها بررسی شود.
طبق اعلام مرکز کنترل و پیشگیری از امراض ایالات متحده (CDC)، شیگلوز توسط گروهی از باکتریها به نام شیگلا ایجاد میشود. در بسیاری از افرادی که به این بیماری مبتلا هستند علائمی مانند اسهال، تب و گرفتگیهای معده بروز مییابد. این در حالی است که برخی افراد هیچ علائمی ندارند. افراد پس از قرار گرفتن در معرض مدفوعِ بیماری که به شیگلوز مبتلا است، در تماس با این باکتری قرار میگیرند.
طبق اعلام این آژانس، شیگلا هر ساله در سراسر جهان باعث کشته شدن حدود ۶۰۰ هزار نفر میشود که عمدتاً به دلیل بهداشت نامناسب و نبود فاضلابها و سرویسهای بهداشتی استاندارد رخ میدهد.
مرکز کنترل و پیشگیری از امراض ایالات متحده توصیه میکند برای پیشگیری از آلوده شدن به شیگلا، دستان خود را به خصوص قبل از خوردن غذا یا آشپزی به دقت با آب و صابون بشویید و بهداشت فردی را به ویژه در ارتباط با افراد آلوده به این عفونت رعایت کنید.
حقایقی عجیب از جانوری که در اعماق زمین زندگی میکنند؟
مجله ایلیاد/ یک گروه تحقیقاتی به رهبری دانشمندان دانشگاه آمریکایی، موفق بهتوالی بندی ژنومِ «هالیسفالوبوس مفیستو» شدند؛ این کِرم گرمادوست از جمله جاندارانی است که در عمیقترین قسمتها زندگی میکند. محققان سازوکارهایی را که طی آن این کرم خود را با شرایط بغرنج و نامساعد وِفق داده است، مورد بررسی قرار دادند.
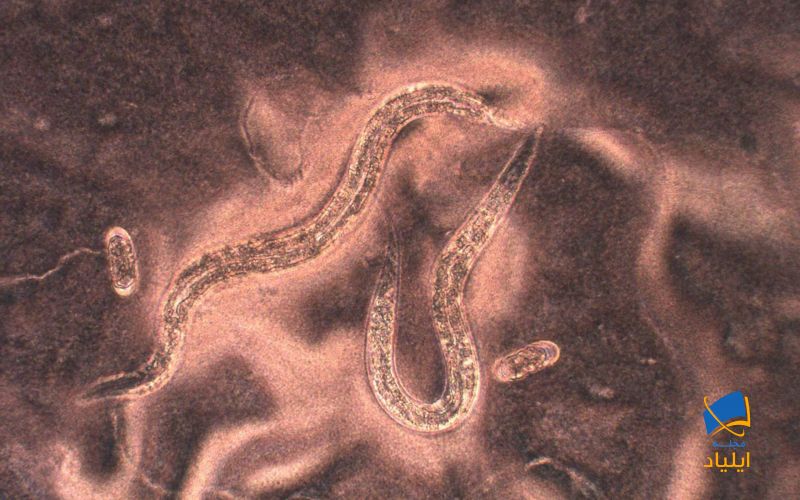
اکتشافات نشان داد که کِرم هالیسفالوبوس مفیستو اصالتاً در آبگیرهای زیرزمینی پُر از سیال سکونت دارد که در معدن طلای بیتریکس آفریقای جنوبی در ۱.۳ کیلومتریِ زیر سطح قابلدسترسی است. اینگونه کرم انگل تنها ۰.۵ میلیمتر طول داشته و در آبهای غنی از متان، داغ و قلیایی با pH معادل ۷.۹ زیست میکند. تاریخنگاری رادیو کربن نشان میدهد که این آبگیر، قدمتی بیش از ۶۰۰۰ سال دارد.
دکتر «جان براشت»، محقق و نویسندهی ارشد مقالهای که در مجله Nature Communications چاپ شده است، اظهار کرد: « هالیسفالوبوس مفیستو نخستین جاندار زیرزمینی است که ژنومش توالی بندی شد. ژنوم این جاندار میتواند با ارائه شواهدی نشان بدهد که حیات چگونه میتواند در زیر سطح زمین تداوم داشته باشد. همچنین، روش جدیدی برای درک چگونگی امکان تداوم حیات در سیارههای دیگر فراهم میکند.»
توالی نشان داد که ژنومِ هالیسفالوبوس مفیستو به طرز عجیبی تعداد کثیری از پروتئینهایHsp70 را رمزگذاری میکند؛ این یافته توجه محققان را به خود جلب کرده، زیرا خیلی از گونههای کرم انگل که ژنومشان توالیبندی شده است، چنین تعداد زیادی از پروتئین فوق را ندارند. Hsp70 ژنی است که بهخوبی موردمطالعه قرارگرفته است و در همه گونههای جانوری وجود دارد و سلامت سلولی را در پی آسیب گرمایی احیا میکند.
بسیاری از ژنهای Hsp70 در ژنومِ هالیسفالوبوس مفیستو نسخههایی از خودشان بودند. این ژنوم نسخههای بیشتری از ژنهای AIG1 را دارد که در گیاهان و حیوانات وجود دارد. دکتر براشت خاطرنشان کرد: «تحقیقات بیشتری در این زمینه موردنیاز است، اما وجود نسخههای این ژن مهر تاییدی بر سازگاری فرگشتی این کِرم است. این کرم نمیتواند جایی فرار کند؛ در زیرزمین است. چارهای بهجز سازگاری با حیات ندارد، وگرنه جانش را از دست میدهد. پیشنهادِ ما این است که وقتی جانداری نمیتواند از گرمای شدید بگریزد، نسخههای بیشتری از این دو ژن تولید میکند تا به بقای خود ادامه بدهد.»
در مقاله دیگری، دکتر براشت و همکارانش چندین ژنوم را بررسی کرده و دریافتند که بسطِ خانوادههای ژنی Hsp70 و AIG1 در دو کپهایها امری رایج است، گروهی از نرم تنان مثل صدف خوراکی، حلزون دو کپهای و صدف باریک دریایی. این جانداران مثل هالیسفالوبوس مفیستو خود را با گرما وفق دادهاند. این مسئله نشان میدهد که الگویِ شناساییشده در هالیسفالوبوس مفیستو شاید در آن دسته از موجودات زندهای که توان گریز از گرمای محیط را ندارند، به وفور دیده شود.
دست از مبارزه با موشهای شهری بردارید!
زومیت/ تلاش ما در مبارزه با موشها با استفاده از سموم جوندهکش میتواند موجب ایجاد جمعیتهای مقاومی از موشها شود.
جاناتان ریچارسون، استاد زیستشناسی دانشگاه ریچموند است. او درمورد موشهای شهری درحال مطالعه است. این مطلب از زبان وی گزارش شده است.

تنها چند ثانیه طول میکشد تا یکی از آنها پیدا شود، و سپس دیگری. همانطور که من حوالی بعدازظهری در پارک کوچکی در شهر نیویورک قدم میزنم، دهها موش را میبینم که در جهات مختلف به سرعت در حال حرکت هستند. آنها درون جویهای آب، زیر بوتهها و در سطلهای زبالهای که حاوی غذاهایی مختلفی برای آنها است، به فعالیت مشغولند. این موشها روی نیمکتهای خالی اطراف پارک جستوخیز میکنند؛ موشهای میدان چرچیل بازگشتهاند.
من به مطالعهی موشهای شهری مشغولم اما این پارک کوچک موجب کنجکاوی من شده است. اولین باری که از میدان دیدن کردم، زمانی بود که در یک گشتوگذار خانوادگی، چندین دقیقه بهدنبال جایی برای نشستن بودم. اما یک بومشناس شهری هیچگاه نسبتبه محیط اطراف خود بیتوجه نیست. من هرگز اینقدر موش را در چنین منطقهی کوچکی ندیده بودم.
بهطور کلی، موشها حیوانات شبگردی هستند، بنابراین احتمالا فعالیت بالای آنها طی روز بهمعنای این است که هجوم آنها شدید است. چیزی که خطر انتقال بیماری به انسان و آسیب به زیرساختهای شهری را افزایش میدهد و حتی روی سلامت روان ساکنان شهر تأثیر منفی دارد. اثرات بهداشتی، اقتصادی و اجتماعی ناشی از هجوم موشها میتواند قابلتوجه باشد.
درحالیکه موشهای صحرایی قهوهای (با نام علمی راتوس نروژیکوس)، برای ساکنان شهر نیویورک ناآشنا نیستند، موشهای میدان چرچیل بسیار زیاد شده بودند. در سالهای بعد، ایستگاههای طعمهی موش در اطراف پارک ظاهر شد. جعبههای سیاه آشنایی که با طعمههای خوراکی حاوی ترکیبات کشندهی جوندگان پر شده بود و تکنسینها آنها را به آسانی طی یک برنامهی زمانی جایگزین میکردند. بهنظر میرسید که این کار بسیار نتیجهبخش بود؛ در آن سال من هیچ موشی در میدان چرچیل ندیدم.
موشها بهسرعت دربرابر وضعیت غذا سازگار میشوند و با تولیدمثل بیشتر، فرزندان کافی برای احیای مجدد جمعیت تولید میکنند. بنابراین با اینکه سالانه میلیونها دلار برای مبارزه با موشها صرف میشود، بهنظر میرسد که تعداد آنها در شهرهای سرتاسر جهان رو به افزایش باشد. بیشتر جمعیتهای موش پس از پایان برنامه کنترل سریعا به حالت اولیه برمیگردند؛ پدیدهای که با عنوان «اثر بومرنگ» شناخته میشود. میدان چرچیل مثالی از این اثر است؛ وقتی ایستگاههای جوندهکش حذف شد، موشها برگشتند.
درحالیکه تقریبا بازگشت موشها حتمی است، من و همکارانم اخیرا متوجه شدیم موشهایی که جمعیت را احیا میکنند، اساسا با موشهایی که قبل از انجام برنامهی دفع موش وجود داشتند، متفاوت هستند. بهعنوان مثال، یک برنامه ریشهکنی فشردهی موشها در سال ۲۰۱۵ در بخشهایی از سالوادور در کشور برزیل موجب شد جمعیت موشها به نصف برسد. درنتیجهی برنامه مذکور، تنوع ژنتیکی درون جمعیت موشها ۹۰ درصد کاهش پیدا کرد. این کاهش شامل از دست رفتن بسیاری از نادرترین واریانتهای ژنی بود. تصور میشود برای اینکه جمعیتی بتواند در محیطهای درحال تغییر پیرامون خود زنده بماند، باید از تنوع ژنتیکی بالایی برخوردار باشد. علاوهبراین، به دلیل اینکه بازماندگان خویشاوندی نزدیکی با هم داشتند، خطر بروز همخونی در میان موشهای باقی مانده بیشتر بود. همهی این تأثیرات مشاهدهشده در موشهای سالوادور وضعیتی هستند که دانشمندان آن را تنگنا یا گلوگاه ژنتیکی میخوانند و با هر استانداردی که درنظر گرفته شود، مورد شدیدی است.
تنگنای ژنتیکی همیشه درمورد جمعیتهای آسیبپذیری که حفاظت از آنها مهم است، مسئلهی نگرانکنندهای بهشمار میرود. در این وضعیت، معمولا بقای گونهی در معرض خطر در بلندمدت به خطر میافتد. اما گونههای آفتی همچون موشهای صحرایی، موش، سوسکها و ساسها در معرض تلاشهای عمدی مکرر در جهت ازبینبردن جمعیت قرار دارند.
مشکل این جا است که معمولا کارکنان مدیریت آفات با شهرها یا دارندگان املاک همکاری ندارند و این برنامهها اغلب در دورههای زمانی کوتاهمدت انجام میشود. این در حالی است که دانشمندان به ردیابی ماندگاری آفات شهری در بلندمدت علاقمند هستند. جورجینا سیلویرا، بهعنوان هماهنگکنندهی بهداشت محیط شهر سامرویل در ماساچوست، در خط مقدم تلاش برای تلفیق مدیریت آفات و تصمیمگیریهای سیاسی، با دیدگاهی علمی و در روندهای طولانیمدت است. سیلویرا خاطرنشان میکند:
بیشتر این شرکا درمورد جمعیت موشها در بلندمدت فکر نمیکنند. در مفهوم عملی، مانند این است که آتشسوزی را با راهحلهای سریع خاموش کنید؛ اغلب به این دلیل که ارتباط کمی بین ساکنان، سازمانهای شهری، متخصصان مدیریت آفات و دانشمندان درمورد اهداف پایدار وجود دارد.

نسل آینده موشهای راتوس نروژیکوس
بقای سازگارترین موشها
برای موشهایی که از برنامهی کنترل آفات جان سالم به در میبرند، دو نتیجه بلندمدت وجود دارد که گروه پژوهشی ما درحال بررسی آن است. نخست و مورد نگرانکننده، ایدهی «بقای اصلح» است. یک برنامهی کنترل موش موفق میتواند بیشتر افراد آن جمعیت را حذف کند. بازماندگان احتمالا دارای صفات خاصی هستند که موجب میشود آنها دربرابر روشهای دفع جوندگان مقاومت کرده و زنده بمانند. این بازماندگان سپس فرزندان زیادی تولید میکنند که صفات مفید آنها را بههمراه دارند. اگر طی یک برنامهی کنترل، تنها سازگارترین موشها زنده بمانند، بازماندگان ممکن است حتی بهتر بتوانند با شرایط شهری کنار آمده و از منابع آن استفاده کنند و جمعیت جدیدی از موشهایی برتر را پدید میآورند که میتوانند تولیدمثل کرده و جمعیت را احیا کنند. درحقیقت، دانشمندان نسخههای خاصی از برخی از ژنها را شناسایی کردهاند که موجب میشود سمومی که برای کشتن جوندگان استفاده میشود، روی موشهای حاوی این واریانتهای ژنی تأثیری نداشته باشد. این واریانتهای ژنی مفید در برخی از جمعیتهای طبیعی موش که مرتبا درمعرض این سموم قرار میگیرند، نیز دیده میشود.
تکامل موشهای بیمارگونه
ازطرف دیگر، زیستشناسان میدانند که ممکن است عواقب منفی شدیدی در انتظار جمعیتهایی باشد که فاقد تنوع ژنتیکی هستند؛ چیزی که مشابه خطرات همخونی در انسان است (ازدواج فامیلی). دادههای سالوادور نشان میدهد که موشها ممکن است بهسرعت طی یک برنامهی کنترل کشنده، بخش زیادی از تنوع ژنتیکی خود را از دست بدهند. این تنوع، کلیدی است که با آنگونهها میتوانند طی انتخاب طبیعی دربرابر تغییرات محیطی پاسخ دهند؛ محیطهای شهری نیز میتوانند به سرعت تغییر کنند.
بنابراین دومین پیامد بلندمدت ممکن برای موشهایی که در معرض برنامههای کنترل مکرر قرار میگیرند، کاهش تدریجی در ماندگاری، تولیدمثل و دیگر صفات مرتبط با شایستگی تکاملی است. این موضوع در کلاغها دیده شده است؛ جایی که همخونی با کاهش ماندگاری و ضعف سیستم ایمنی همراه بوده است. موشهایی که بهتدریج ضعیف و بیمارتر میشوند، مطمئنا سناریوی برتر در مبارزه با هجوم مداوم موشها هستند.
بنابراین برای موشهای میدان چرچیل، سالوادور و دیگر مکانهایی که در آنها بهطور مداوم برنامههای کنترل اجرا میشود، چه اتفاقی میافتد؟
گروه پژوهشی ما برای درک این موضوع که آیا موشها به سمت ایجاد مجموعهای از صفات فوقالعاده یا صفات بیمار پیش میروند، درحال مطالعهی جمعیتها قبل و پس از اجرای برنامههای کنترل است
تا مشخص شود که چگونه ماندگاری، تولیدمثل و دیگر صفات سودمند در جریان این برنامههای کنترل تغییر پیدا میکنند.

جاناتان ریچاردسون درحال وزن کردن یک موش بهعنوان قسمتی از مطالعهی موشها در نیویورک
اما مطالعهی این جنبهها از زیستشناسی موشها، در جمعیتهای وحشی و مخصوصا در محیطها شهری بسیار چالشبرانگیز است. شاید با استفاده از ابزارهای ژنتیکی بتوان عملیترین راهها را برای ارزیابی اثربخشی برنامههای کنترل پیدا کرد و روش استانداردی را ایجاد کرد که در سرتاسر جهان قابل استفاده باشد.
ما میدانیم که کنترل موشهای شهری باید چیزی فراتر از فقط مسموم کردن آنها باشد. کنترل جامع جوندگان به تمرکز بر اهداف بلندمدت و پایدار، کاهش جمعیتها تا سطح قابل تحمل با استفاده از ابزارهای مختلفی مانند جوندهکشها، یخ خشک و حتی استفاده از داروهایی برای کاهش باروری، نیاز دارد. البته سادهترین و مؤثرترین روش، کاهش دسترسی به زبالهها و نصب سطلهای زبالهی ضدجونده است. در همین حین، پژوهشها میتوانند مشخص کنند که این همه پول و تلاش چه تأثیری روی آفات شهری دارد؛ آیا درحال کاهش قابلیت زندهمانی آنها هستیم یا به تکامل کمک میکنیم تا موشهایی با خصوصیات برتر ایجاد کند.